近日,中国医药质量管理协会发布《研究者发起的抗肿瘤体细胞临床研究细胞制剂制备和质量控制规范》(T/CQAP 3014—2024)标准(以下简称“标准”),并于2024年5月1日正式实施。
该标准旨在制定适应中国国情、符合企业实际、标准统一规范的抗肿瘤体细胞临床研究质量控制体系。由来自于17家单位的22位行业专家共同完成,包括中山大学肿瘤防治中心、中国医药质量管理协会、广东省药品检验所等。泛恩生物作为实体肿瘤免疫细胞治疗的自主创新企业,受邀参与了该标准的制定,为本行业未来发展提出了意见和建议,共同推动我国抗肿瘤细胞临床研究高质量发展。
标准的主要技术内容规定了在研究者发起的抗肿瘤体细胞临床研究中细胞制剂的分类,细胞制剂制备,细胞制剂质量控制要求,细胞制剂的临床前研究,细胞制剂的放行质量控制要求、标签、包装、运输、贮存及不合格和剩余细胞制剂的处理等。
泛恩生物坚持自主研发和原始创新、拥有多项细胞免疫治疗核心技术。未来,泛恩生物将会进一步助推中国细胞治疗临床研究相关工作的规范化、标准化、科学化及中国细胞治疗相关技术高质量发展。
关于泛恩
广州泛恩生物科技有限公司由国家“海外高层次人才引进计划”、广东省“珠江人才”、广州开发区“领军人才”等人才团队创立,专注于实体肿瘤的免疫细胞治疗药物开发。公司突破了实体肿瘤免疫治疗的多个关键技术瓶颈,拥有自体肿瘤抗原特异TCR快速鉴定、多基因逆转实体肿瘤微环境、免疫治疗有效患者准确筛选等多项前沿核心技术。自主研制了:世界首创个体化TCR-T细胞治疗、多款逆转实体肿瘤微环境的TCR/CAR-T细胞治疗、高度富集肿瘤抗原特异T细胞的TAL-T与TIL细胞治疗、下一代体内递送TCR/CAR-T细胞治疗等有效治疗实体肿瘤的细胞治疗产品。
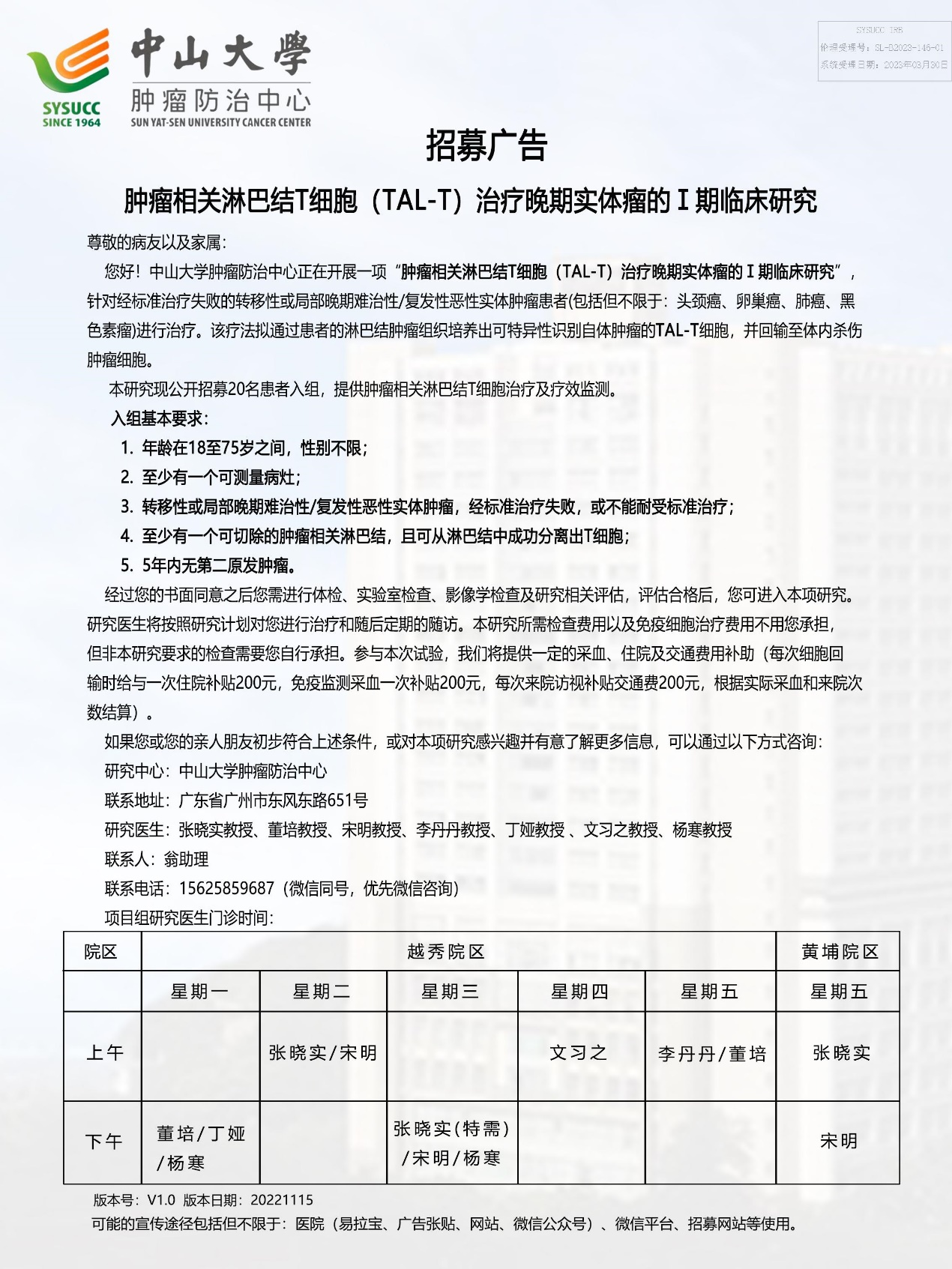
泛恩生物以Tas T细胞为基础,研制了个体化TCR-T和TAL-T两个细胞治疗方法,适用于大部分实体肿瘤患者。目前正在开展晚期实体肿瘤I期临床研究,详情见患者招募信息。如果您想了解更多信息,请联系临床研究助理:翁先生,1562859687,微信同号。